医药资讯
-
 双相情感障碍遗传学的新发现:HECTD2与AKAP11基因突变的关联 双相情感障碍(BD)是一种遗传性强的精神障碍,研究表明其遗传性高达60%-85%。尽管多项全基因组关联研究(GWAS)已经揭示了与双相情感障碍相关的常见遗传变异,但这些变异仅能解释约20%的遗传性。最近,安进研究团队利用冰岛与英国生物库的数据,对双相情感障碍的罕见基因突变进行了深入分析,并取得了突破性进展。 罕见基因变异与双相情感障碍的关联 研究团队通过分析冰岛生物库(ICE)和英国生物库(UKB)的数据,发现了与双相情感障碍相关的罕见功能丧失突变。这些数据涉及超过58,000名冰岛居民和超过42万名英国或爱尔兰居民的全基因组测序。研究重点聚焦于13768个基因的功能丧失变异与双相情感障碍的关系。 通过对两项数据集的综合分析,研究发现HECTD2基因中的罕见功能丧失变异与双相情感障碍显著相关。携带这种基因变异的个体,患病的风险增加了810%(OR=9.1,p=4.7×10^-7)。这一发现得到了BipEx研究的验证,进一步证明了HECTD2与双相情感障碍之间的密切关系(p=4.1×10^-8)。 此外,AKAP11基因也被发现与双相情感障碍相关。研究显示,在ICE-UKB数据集中的38种AKAP11功能丧失变异中,共有76名携带者,且携带者的患病风险增加了1080%(OR=11.8,p=7.4×10^-9)。 认知功能与基因变异的关系 研究进一步发现,双相情感障碍患者的认知表现普遍低于健康对照群体。特别是,HECTD2基因的功能丧失变异与认知能力的下降相关联(效应值=-0.38,p=0.030)。值得注意的是,即使在未确诊为双相情感障碍的个体中,携带HECTD2功能丧失变异的个体,其认知水平也可能低于非携带者。 虽然AKAP11基因的认知数据尚不充分,但研究认为,HECTD2与认知能力之间的关联值得进一步研究,以便更好地理解其在双相情感障碍中的作用。 关联分析与共病因素的排除 研究排除了合并精神分裂症或分裂情感性障碍的患者,结果仍然表明HECTD2和AKAP11基因的功能丧失变异与双相情感障碍的关系显著,说明这些基因变异与双相情感障碍的关联主要由双相情感障碍本身驱动,而非其他共病症状(如焦虑或抑郁)所影响。 与锂盐治疗的潜在关联 在双相情感障碍的药物治疗中,锂盐被广泛应用,并被认为可以有效降低患者的住院风险。研究发现,HECTD2和AKAP11基因与锂盐的靶点GSK3β密切相关,这为进一步研究锂盐的作用机制提供了新的线索。通过对这些基因的功能研究,可能揭示出GSK3β、HECTD2与AKAP11之间的生物学联系,为双相情感障碍的治疗提供新的理论基础。 总结 本项研究揭示了HECTD2和AKAP11基因的功能丧失变异与双相情感障碍的显著关联,为双相情感障碍的遗传机制研究提供了新的视角。这些发现不仅为早期诊断提供了潜在的生物标志物,还为进一步开发靶向治疗提供了新的方向。随着研究的深入,未来有望通过精准的遗传筛查与个性化治疗,帮助改善双相情感障碍患者的预后。
双相情感障碍遗传学的新发现:HECTD2与AKAP11基因突变的关联 双相情感障碍(BD)是一种遗传性强的精神障碍,研究表明其遗传性高达60%-85%。尽管多项全基因组关联研究(GWAS)已经揭示了与双相情感障碍相关的常见遗传变异,但这些变异仅能解释约20%的遗传性。最近,安进研究团队利用冰岛与英国生物库的数据,对双相情感障碍的罕见基因突变进行了深入分析,并取得了突破性进展。 罕见基因变异与双相情感障碍的关联 研究团队通过分析冰岛生物库(ICE)和英国生物库(UKB)的数据,发现了与双相情感障碍相关的罕见功能丧失突变。这些数据涉及超过58,000名冰岛居民和超过42万名英国或爱尔兰居民的全基因组测序。研究重点聚焦于13768个基因的功能丧失变异与双相情感障碍的关系。 通过对两项数据集的综合分析,研究发现HECTD2基因中的罕见功能丧失变异与双相情感障碍显著相关。携带这种基因变异的个体,患病的风险增加了810%(OR=9.1,p=4.7×10^-7)。这一发现得到了BipEx研究的验证,进一步证明了HECTD2与双相情感障碍之间的密切关系(p=4.1×10^-8)。 此外,AKAP11基因也被发现与双相情感障碍相关。研究显示,在ICE-UKB数据集中的38种AKAP11功能丧失变异中,共有76名携带者,且携带者的患病风险增加了1080%(OR=11.8,p=7.4×10^-9)。 认知功能与基因变异的关系 研究进一步发现,双相情感障碍患者的认知表现普遍低于健康对照群体。特别是,HECTD2基因的功能丧失变异与认知能力的下降相关联(效应值=-0.38,p=0.030)。值得注意的是,即使在未确诊为双相情感障碍的个体中,携带HECTD2功能丧失变异的个体,其认知水平也可能低于非携带者。 虽然AKAP11基因的认知数据尚不充分,但研究认为,HECTD2与认知能力之间的关联值得进一步研究,以便更好地理解其在双相情感障碍中的作用。 关联分析与共病因素的排除 研究排除了合并精神分裂症或分裂情感性障碍的患者,结果仍然表明HECTD2和AKAP11基因的功能丧失变异与双相情感障碍的关系显著,说明这些基因变异与双相情感障碍的关联主要由双相情感障碍本身驱动,而非其他共病症状(如焦虑或抑郁)所影响。 与锂盐治疗的潜在关联 在双相情感障碍的药物治疗中,锂盐被广泛应用,并被认为可以有效降低患者的住院风险。研究发现,HECTD2和AKAP11基因与锂盐的靶点GSK3β密切相关,这为进一步研究锂盐的作用机制提供了新的线索。通过对这些基因的功能研究,可能揭示出GSK3β、HECTD2与AKAP11之间的生物学联系,为双相情感障碍的治疗提供新的理论基础。 总结 本项研究揭示了HECTD2和AKAP11基因的功能丧失变异与双相情感障碍的显著关联,为双相情感障碍的遗传机制研究提供了新的视角。这些发现不仅为早期诊断提供了潜在的生物标志物,还为进一步开发靶向治疗提供了新的方向。随着研究的深入,未来有望通过精准的遗传筛查与个性化治疗,帮助改善双相情感障碍患者的预后。2025-03-31
-
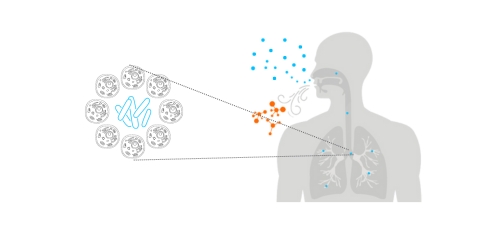 呼气VOC分子筛查结核病:加速终结结核病的关键技术 结核病(TB)依然是全球公共卫生的重大挑战。尽管现有的检测方法可以判断结核分枝杆菌是否存在,但其对传染性结核病的诊断仍然存在一定局限性。因此,研发便捷、高效、无创的筛查工具显得尤为迫切。呼气挥发性有机化合物(VOC)分析作为一种新兴的非侵入性筛查方法,因其快速、便捷等优势,正成为结核病早期诊断的研究热点。 结核病现状与诊断挑战 2023年,全球新增结核病病例达1040万,且每年因结核病死亡的患者高达140万,结核病依然是全球主要的传染病杀手。现有的结核病诊断手段,如血液检测,虽然能确诊是否感染结核分枝杆菌,但无法判定患者是否为传染性结核病患者。进一步的检查手段,如胸部X光、CT扫描和细菌培养,成本高、技术要求复杂,且在资源匮乏地区难以普及。此外,这些检查可能会给患者带来身体上的不适。 世界卫生组织(WHO)强调,急需一种快速、无创的筛查工具,能够有效缩短诊断时间,减少结核病的传播风险。 呼气VOC标志物的发现与验证 2007年,美国Phillips团队在结核分枝杆菌的培养物中首次发现了130种特异性挥发性有机化合物(VOC),包括苯、萘及其衍生物。通过对临床样本的分析,研究团队验证了这些VOC标志物在区分结核病患者与健康人群中的潜力,准确率达到了84%的敏感性与64.7%的特异性。 2010年,研究团队进一步将氧化应激标志物与VOC标志物结合,使诊断准确性提升至85%,但特异性仍然较低,提示需要进一步优化标志物的组合。 2023年,《BMC Infectious Diseases》期刊发布了一项横断面研究,分析了518名结核病患者和887名对照者的VOC,并通过机器学习构建了诊断模型。在430个盲测样本中,该模型显示出92.6%的准确率、91.7%的敏感性、93.0%的特异性,AUC值为0.975,且不受患者年龄、性别或是否接受抗结核治疗的影响。 2025年,发表在《科学报告》上的最新研究首次报告了邻伞花烃等新型VOC标志物,可有效区分活动性结核与耐药性结核。这一发现极大地缩短了诊断周期,从几周缩短至数小时,为全球减少结核病相关死亡提供了新契机。 呼气VOC检测的技术优势 无创性 :呼气VOC分析技术是一种无创性检测方法,因其不需要侵入式操作,更容易为患者接受,尤其对儿童、老年人和孕妇等特殊人群友好。 快速检测 :与传统的检查方法相比,呼气VOC检测只需几分钟即可完成,适合大规模筛查,尤其适用于疫情防控和基层医疗。 动态监测 :VOC分析不仅能用于结核病的诊断,还可以用于治疗过程中动态监测疾病进展,尤其在耐药性结核等复杂病例的监测中具有潜力。 直接性 :结核病主要侵袭肺部,呼气中的VOC能直接反映肺部的病变情况,诊断更为精准。 行业发展与政策支持 国际资金与科研投入 盖茨基金会已累计投入650万美元支持呼气VOC技术的研发,其中150万美元专门用于结核病早期诊断的研究。这种资金支持将推动更多创新技术的诞生,并促进呼气VOC检测技术在结核病筛查中的应用。 国家政策与技术突破 《全国结核病防治规划(2024-2030年)》明确将创新诊断技术列为优先发展领域,鼓励开发便携式设备,提高诊断效率。随着呼气VOC分析技术的不断成熟,这项技术有望在结核病防治工作中发挥重要作用,尤其是在资源匮乏地区。 呼气VOC技术的未来前景 随着技术的不断进步,呼气VOC分析不仅有望加速结核病的早期诊断,减轻患者的经济和心理负担,还能够有效控制结核病的传播,最终帮助终结这一全球性的公共卫生危机。
呼气VOC分子筛查结核病:加速终结结核病的关键技术 结核病(TB)依然是全球公共卫生的重大挑战。尽管现有的检测方法可以判断结核分枝杆菌是否存在,但其对传染性结核病的诊断仍然存在一定局限性。因此,研发便捷、高效、无创的筛查工具显得尤为迫切。呼气挥发性有机化合物(VOC)分析作为一种新兴的非侵入性筛查方法,因其快速、便捷等优势,正成为结核病早期诊断的研究热点。 结核病现状与诊断挑战 2023年,全球新增结核病病例达1040万,且每年因结核病死亡的患者高达140万,结核病依然是全球主要的传染病杀手。现有的结核病诊断手段,如血液检测,虽然能确诊是否感染结核分枝杆菌,但无法判定患者是否为传染性结核病患者。进一步的检查手段,如胸部X光、CT扫描和细菌培养,成本高、技术要求复杂,且在资源匮乏地区难以普及。此外,这些检查可能会给患者带来身体上的不适。 世界卫生组织(WHO)强调,急需一种快速、无创的筛查工具,能够有效缩短诊断时间,减少结核病的传播风险。 呼气VOC标志物的发现与验证 2007年,美国Phillips团队在结核分枝杆菌的培养物中首次发现了130种特异性挥发性有机化合物(VOC),包括苯、萘及其衍生物。通过对临床样本的分析,研究团队验证了这些VOC标志物在区分结核病患者与健康人群中的潜力,准确率达到了84%的敏感性与64.7%的特异性。 2010年,研究团队进一步将氧化应激标志物与VOC标志物结合,使诊断准确性提升至85%,但特异性仍然较低,提示需要进一步优化标志物的组合。 2023年,《BMC Infectious Diseases》期刊发布了一项横断面研究,分析了518名结核病患者和887名对照者的VOC,并通过机器学习构建了诊断模型。在430个盲测样本中,该模型显示出92.6%的准确率、91.7%的敏感性、93.0%的特异性,AUC值为0.975,且不受患者年龄、性别或是否接受抗结核治疗的影响。 2025年,发表在《科学报告》上的最新研究首次报告了邻伞花烃等新型VOC标志物,可有效区分活动性结核与耐药性结核。这一发现极大地缩短了诊断周期,从几周缩短至数小时,为全球减少结核病相关死亡提供了新契机。 呼气VOC检测的技术优势 无创性 :呼气VOC分析技术是一种无创性检测方法,因其不需要侵入式操作,更容易为患者接受,尤其对儿童、老年人和孕妇等特殊人群友好。 快速检测 :与传统的检查方法相比,呼气VOC检测只需几分钟即可完成,适合大规模筛查,尤其适用于疫情防控和基层医疗。 动态监测 :VOC分析不仅能用于结核病的诊断,还可以用于治疗过程中动态监测疾病进展,尤其在耐药性结核等复杂病例的监测中具有潜力。 直接性 :结核病主要侵袭肺部,呼气中的VOC能直接反映肺部的病变情况,诊断更为精准。 行业发展与政策支持 国际资金与科研投入 盖茨基金会已累计投入650万美元支持呼气VOC技术的研发,其中150万美元专门用于结核病早期诊断的研究。这种资金支持将推动更多创新技术的诞生,并促进呼气VOC检测技术在结核病筛查中的应用。 国家政策与技术突破 《全国结核病防治规划(2024-2030年)》明确将创新诊断技术列为优先发展领域,鼓励开发便携式设备,提高诊断效率。随着呼气VOC分析技术的不断成熟,这项技术有望在结核病防治工作中发挥重要作用,尤其是在资源匮乏地区。 呼气VOC技术的未来前景 随着技术的不断进步,呼气VOC分析不仅有望加速结核病的早期诊断,减轻患者的经济和心理负担,还能够有效控制结核病的传播,最终帮助终结这一全球性的公共卫生危机。2025-03-31
-
 华润三九发布999益气清肺颗粒,推动呼吸健康新纪元 首个中药3.2类新药亮相 3月28日,在“第一届中药产业互联互通大会”上,华润三九推出了首个中药3.2类新药——999益气清肺颗粒。该药由华润三九与中国工程院院士张伯礼及其科研团队联合研发,是专为呼吸道感染康复期患者设计的创新型中药,并且已获得国家药监局批准上市。 中医药现代化的责任与担当 999益气清肺颗粒的发布,标志着华润三九在呼吸品类的产品布局迈出了新的一步,也彰显了公司推动中医药现代化的责任感和使命感。华润三九副总裁王亮与张伯礼院士共同按下启动键,宣布新药正式面世。 呼吸道感染康复期的市场空白 随着甲流、支原体肺炎等呼吸道疾病的频繁爆发,呼吸道感染已成为继肿瘤、心血管疾病和糖尿病之后,严重危害人类健康的疾病之一。尽管对呼吸道感染的预防和治疗已有一定研究,但康复期的治疗却一直未受到足够的关注,且市面上缺乏有效的药物解决方案。 999益气清肺颗粒的中药基础 张伯礼院士指出,很多患者在病毒感染转阴后,机体并未完全恢复。从中医的角度看,这种情况属于“邪气已去,正气未复”。基于这一理论,张伯礼及其团队结合经典方剂生脉散和平胃散,加以现代化调整,研发出了999益气清肺颗粒。该药主要通过益气养阴、健脾和中的方式,有效缓解呼吸道感染康复期的常见症状,如乏力、气短和干咳少痰等。 临床研究证实效果显著 999益气清肺颗粒的处方源自张伯礼院士2020年提出的“清金益气方”,该方剂在华润三九和多家医院的临床试验中得到了广泛验证。天津中医药大学第一附属医院等多个医院进行的多中心、随机、双盲、平行对照的临床试验表明,患者在服药14天后,干咳、乏力、气短等症状的改善显著,且其疗效在临床治疗中得到了充分验证。 为广泛人群提供治疗方案 张伯礼院士强调,999益气清肺颗粒是一款结合中医理论、临床经验与现代研究的创新药物,适用于广泛的人群。华润三九党委书记、董事长邱华伟表示,公司致力于传承中医药价值,并通过创新研发,提供更多安全有效的治疗选择,帮助广大患者更便捷地进行呼吸道疾病康复。 战略意义:全面布局呼吸健康市场 华润三九副总裁王亮在发布会上表示,999益气清肺颗粒的发布,标志着公司在呼吸健康领域实现了从预防、治疗到康复的全周期覆盖。这一创新药物的推出,不仅填补了市场空白,也为华润三九的呼吸品类布局注入了新的动力。 未来展望:多元化创新与质量发展 华润三九将继续围绕中医药产业链的创新与布局,打造更多高品质药品,推动中医药现代化高质量发展。未来,公司将进一步加强对消费者健康的关爱,为广大消费者提供更精准、有效的用药方案,推动“健康中国”战略的实施。 结语:呼吸健康的新选择 999益气清肺颗粒的发布,不仅是华润三九在呼吸健康领域的一次重大突破,也为消费者提供了康复期呼吸道疾病治疗的新选择。随着该药的上市,更多呼吸道感染患者将受益于这一创新药物,为健康管理带来新的希望。
华润三九发布999益气清肺颗粒,推动呼吸健康新纪元 首个中药3.2类新药亮相 3月28日,在“第一届中药产业互联互通大会”上,华润三九推出了首个中药3.2类新药——999益气清肺颗粒。该药由华润三九与中国工程院院士张伯礼及其科研团队联合研发,是专为呼吸道感染康复期患者设计的创新型中药,并且已获得国家药监局批准上市。 中医药现代化的责任与担当 999益气清肺颗粒的发布,标志着华润三九在呼吸品类的产品布局迈出了新的一步,也彰显了公司推动中医药现代化的责任感和使命感。华润三九副总裁王亮与张伯礼院士共同按下启动键,宣布新药正式面世。 呼吸道感染康复期的市场空白 随着甲流、支原体肺炎等呼吸道疾病的频繁爆发,呼吸道感染已成为继肿瘤、心血管疾病和糖尿病之后,严重危害人类健康的疾病之一。尽管对呼吸道感染的预防和治疗已有一定研究,但康复期的治疗却一直未受到足够的关注,且市面上缺乏有效的药物解决方案。 999益气清肺颗粒的中药基础 张伯礼院士指出,很多患者在病毒感染转阴后,机体并未完全恢复。从中医的角度看,这种情况属于“邪气已去,正气未复”。基于这一理论,张伯礼及其团队结合经典方剂生脉散和平胃散,加以现代化调整,研发出了999益气清肺颗粒。该药主要通过益气养阴、健脾和中的方式,有效缓解呼吸道感染康复期的常见症状,如乏力、气短和干咳少痰等。 临床研究证实效果显著 999益气清肺颗粒的处方源自张伯礼院士2020年提出的“清金益气方”,该方剂在华润三九和多家医院的临床试验中得到了广泛验证。天津中医药大学第一附属医院等多个医院进行的多中心、随机、双盲、平行对照的临床试验表明,患者在服药14天后,干咳、乏力、气短等症状的改善显著,且其疗效在临床治疗中得到了充分验证。 为广泛人群提供治疗方案 张伯礼院士强调,999益气清肺颗粒是一款结合中医理论、临床经验与现代研究的创新药物,适用于广泛的人群。华润三九党委书记、董事长邱华伟表示,公司致力于传承中医药价值,并通过创新研发,提供更多安全有效的治疗选择,帮助广大患者更便捷地进行呼吸道疾病康复。 战略意义:全面布局呼吸健康市场 华润三九副总裁王亮在发布会上表示,999益气清肺颗粒的发布,标志着公司在呼吸健康领域实现了从预防、治疗到康复的全周期覆盖。这一创新药物的推出,不仅填补了市场空白,也为华润三九的呼吸品类布局注入了新的动力。 未来展望:多元化创新与质量发展 华润三九将继续围绕中医药产业链的创新与布局,打造更多高品质药品,推动中医药现代化高质量发展。未来,公司将进一步加强对消费者健康的关爱,为广大消费者提供更精准、有效的用药方案,推动“健康中国”战略的实施。 结语:呼吸健康的新选择 999益气清肺颗粒的发布,不仅是华润三九在呼吸健康领域的一次重大突破,也为消费者提供了康复期呼吸道疾病治疗的新选择。随着该药的上市,更多呼吸道感染患者将受益于这一创新药物,为健康管理带来新的希望。2025-03-31
-
 Lexicon制药与诺和诺德达成独家许可协议,共同开发LX9851治疗肥胖症 2025年3月28日,Lexicon Pharmaceuticals宣布已与全球知名制药公司诺和诺德达成了一项独家许可协议,合作开发LX9851——一种用于治疗肥胖症及其相关代谢紊乱的创新口服药物。这一合作协议为Lexicon带来了高达7500万美元的首付款,并包含潜在的开发、监管和销售里程碑付款,以及LX9851净销售额的分级特许权使用费,总交易价值可能高达10亿美元。 LX9851:创新的口服药物 LX9851是一种高效且选择性的口服小分子抑制剂,其靶点为酰基辅酶A合成酶5(ACSL5)。该酶在脂肪积累和能量平衡的调控中扮演着关键角色。研究显示,LX9851不仅能有效调节脂肪代谢,还可能通过激活回肠制动机制,延缓胃排空并抑制食欲,从而帮助患者增加饱腹感,控制体重。 临床前数据揭示其独特优势 在2024年肥胖症大会上公布的临床前数据中,LX9851与现有抗肥胖药物司美格鲁肽联合使用时,显示出显著的体重减轻效果。相比单独使用司美格鲁肽,联合用药能够显著降低体重、食物摄入量和脂肪量,并在停用司美格鲁肽后,使用LX9851可有效减轻体重反弹。此外,LX9851还对肝脏脂肪变性产生了积极影响,表明其在治疗肥胖症及相关代谢疾病方面的潜力。 合作条款与诺和诺德的角色 根据协议条款,诺和诺德将拥有LX9851在全球范围内所有适应症的独家开发、生产和商业化权利。Lexicon将继续负责完成临床试验申请(IND)相关支持,而诺和诺德则将负责后续的IND申请、药物开发、生产以及市场推广等工作。 Lexicon首席执行官评论合作 Lexicon的首席执行官兼董事Mike Exton博士表示:“此次与诺和诺德的合作不仅为我们带来了可观的资金支持,也显著改善了公司的财务状况。这使我们能够进一步投资并加速现有研发管线的推进,推动公司走向更广阔的未来。” 诺和诺德对合作的期待 诺和诺德糖尿病、肥胖症和MASH(代谢性脂肪性肝病)治疗领域的高级副总裁Jacob Sten Petersen表示:“我们始终致力于满足肥胖症及其他代谢性疾病患者的多样化需求,此次与Lexicon的合作为我们提供了一个探索新生物学机制和治疗方式的机会。我们期待在Lexicon已有的研究基础上,进一步推动LX9851的开发进程。” 未来展望 此次合作将推动LX9851的发展,为肥胖症患者提供一种新的治疗选择。随着肥胖症和相关代谢疾病的患病率逐年上升,LX9851的市场潜力巨大,未来可能为这一领域带来显著的突破。
Lexicon制药与诺和诺德达成独家许可协议,共同开发LX9851治疗肥胖症 2025年3月28日,Lexicon Pharmaceuticals宣布已与全球知名制药公司诺和诺德达成了一项独家许可协议,合作开发LX9851——一种用于治疗肥胖症及其相关代谢紊乱的创新口服药物。这一合作协议为Lexicon带来了高达7500万美元的首付款,并包含潜在的开发、监管和销售里程碑付款,以及LX9851净销售额的分级特许权使用费,总交易价值可能高达10亿美元。 LX9851:创新的口服药物 LX9851是一种高效且选择性的口服小分子抑制剂,其靶点为酰基辅酶A合成酶5(ACSL5)。该酶在脂肪积累和能量平衡的调控中扮演着关键角色。研究显示,LX9851不仅能有效调节脂肪代谢,还可能通过激活回肠制动机制,延缓胃排空并抑制食欲,从而帮助患者增加饱腹感,控制体重。 临床前数据揭示其独特优势 在2024年肥胖症大会上公布的临床前数据中,LX9851与现有抗肥胖药物司美格鲁肽联合使用时,显示出显著的体重减轻效果。相比单独使用司美格鲁肽,联合用药能够显著降低体重、食物摄入量和脂肪量,并在停用司美格鲁肽后,使用LX9851可有效减轻体重反弹。此外,LX9851还对肝脏脂肪变性产生了积极影响,表明其在治疗肥胖症及相关代谢疾病方面的潜力。 合作条款与诺和诺德的角色 根据协议条款,诺和诺德将拥有LX9851在全球范围内所有适应症的独家开发、生产和商业化权利。Lexicon将继续负责完成临床试验申请(IND)相关支持,而诺和诺德则将负责后续的IND申请、药物开发、生产以及市场推广等工作。 Lexicon首席执行官评论合作 Lexicon的首席执行官兼董事Mike Exton博士表示:“此次与诺和诺德的合作不仅为我们带来了可观的资金支持,也显著改善了公司的财务状况。这使我们能够进一步投资并加速现有研发管线的推进,推动公司走向更广阔的未来。” 诺和诺德对合作的期待 诺和诺德糖尿病、肥胖症和MASH(代谢性脂肪性肝病)治疗领域的高级副总裁Jacob Sten Petersen表示:“我们始终致力于满足肥胖症及其他代谢性疾病患者的多样化需求,此次与Lexicon的合作为我们提供了一个探索新生物学机制和治疗方式的机会。我们期待在Lexicon已有的研究基础上,进一步推动LX9851的开发进程。” 未来展望 此次合作将推动LX9851的发展,为肥胖症患者提供一种新的治疗选择。随着肥胖症和相关代谢疾病的患病率逐年上升,LX9851的市场潜力巨大,未来可能为这一领域带来显著的突破。2025-03-29
-
 新研究发现TIM-3诱饵可提升CAR-T细胞治疗B-ALL的效果 B细胞急性淋巴细胞白血病(B-ALL)是一种严重的癌症,通常会影响儿童,是最常见的儿童癌症之一,约占所有儿科癌症的35%。虽然CAR-T细胞疗法在B-ALL的治疗中显示出显著的潜力,但复发问题仍然困扰着许多患者。新的研究揭示了通过可分泌TIM-3诱饵增强CAR-T细胞疗法效果的潜力,为应对这一挑战提供了新的思路。 CAR-T细胞疗法中的复发难题 CAR-T细胞疗法的原理是提取患者体内的T细胞,在实验室中进行改造,使其能够特异性识别并杀死癌细胞。然而,对于B-ALL患者而言,尽管CAR-T细胞在初期能够显著提高患者的生存率,但超过50%的患者在治疗后会复发,这主要归因于B-ALL肿瘤细胞的逃逸机制。 B-ALL如何“关闭”CAR-T细胞 研究人员发现,B-ALL复发细胞中具有较高水平的galectin-9,这是一种参与免疫检查点系统的蛋白质。与此同时,CAR-T细胞表面表达高水平的TIM-3,TIM-3是一个受体,通常与galectin-9结合,从而抑制免疫反应。这一机制使得B-ALL细胞能够通过与CAR-T细胞的TIM-3受体相互作用来关闭CAR-T细胞的免疫功能,从而避免被攻击。 TIM-3诱饵的创新解决方案 为了破解这一免疫逃逸机制,研究人员开发了一种TIM-3诱饵——TIM-3蛋白的可溶性版本,能够有效阻止TIM-3和galectin-9的结合。这种诱饵可以解除B-ALL细胞的免疫逃逸功能,增强CAR-T细胞的抗白血病效果。 实验室中的突破性结果 在小鼠实验中,研究人员将TIM-3诱饵与CAR-T细胞结合,结果显示经过基因改造并能分泌TIM-3诱饵的CAR-T细胞表现出了更强的抗B-ALL效果,并且具有更长久的治疗效果。这一发现为CAR-T疗法的进一步优化和抗复发能力的提高提供了重要的支持。 临床前阶段的前景与未来展望 尽管该研究目前仍处于临床前阶段,但其成果为CAR-T细胞疗法的改进开辟了新的方向。研究者表示,TIM-3诱饵的引入不仅可能减少CAR-T细胞疗法中的复发风险,还可能为未来的“装甲CAR-T细胞”提供理论依据。更重要的是,这项技术有望扩展CAR-T细胞疗法在治疗其他类型的实体瘤中的潜力。 总结 这项研究为提升B-ALL患者的治疗效果提供了新的思路,通过可分泌的TIM-3诱饵来增强CAR-T细胞疗法的抗肿瘤能力,显著减少了复发的可能性。随着进一步的临床试验和研究,这一创新方法有望为更多癌症患者带来福音,特别是在应对B-ALL和实体瘤的治疗挑战时。
新研究发现TIM-3诱饵可提升CAR-T细胞治疗B-ALL的效果 B细胞急性淋巴细胞白血病(B-ALL)是一种严重的癌症,通常会影响儿童,是最常见的儿童癌症之一,约占所有儿科癌症的35%。虽然CAR-T细胞疗法在B-ALL的治疗中显示出显著的潜力,但复发问题仍然困扰着许多患者。新的研究揭示了通过可分泌TIM-3诱饵增强CAR-T细胞疗法效果的潜力,为应对这一挑战提供了新的思路。 CAR-T细胞疗法中的复发难题 CAR-T细胞疗法的原理是提取患者体内的T细胞,在实验室中进行改造,使其能够特异性识别并杀死癌细胞。然而,对于B-ALL患者而言,尽管CAR-T细胞在初期能够显著提高患者的生存率,但超过50%的患者在治疗后会复发,这主要归因于B-ALL肿瘤细胞的逃逸机制。 B-ALL如何“关闭”CAR-T细胞 研究人员发现,B-ALL复发细胞中具有较高水平的galectin-9,这是一种参与免疫检查点系统的蛋白质。与此同时,CAR-T细胞表面表达高水平的TIM-3,TIM-3是一个受体,通常与galectin-9结合,从而抑制免疫反应。这一机制使得B-ALL细胞能够通过与CAR-T细胞的TIM-3受体相互作用来关闭CAR-T细胞的免疫功能,从而避免被攻击。 TIM-3诱饵的创新解决方案 为了破解这一免疫逃逸机制,研究人员开发了一种TIM-3诱饵——TIM-3蛋白的可溶性版本,能够有效阻止TIM-3和galectin-9的结合。这种诱饵可以解除B-ALL细胞的免疫逃逸功能,增强CAR-T细胞的抗白血病效果。 实验室中的突破性结果 在小鼠实验中,研究人员将TIM-3诱饵与CAR-T细胞结合,结果显示经过基因改造并能分泌TIM-3诱饵的CAR-T细胞表现出了更强的抗B-ALL效果,并且具有更长久的治疗效果。这一发现为CAR-T疗法的进一步优化和抗复发能力的提高提供了重要的支持。 临床前阶段的前景与未来展望 尽管该研究目前仍处于临床前阶段,但其成果为CAR-T细胞疗法的改进开辟了新的方向。研究者表示,TIM-3诱饵的引入不仅可能减少CAR-T细胞疗法中的复发风险,还可能为未来的“装甲CAR-T细胞”提供理论依据。更重要的是,这项技术有望扩展CAR-T细胞疗法在治疗其他类型的实体瘤中的潜力。 总结 这项研究为提升B-ALL患者的治疗效果提供了新的思路,通过可分泌的TIM-3诱饵来增强CAR-T细胞疗法的抗肿瘤能力,显著减少了复发的可能性。随着进一步的临床试验和研究,这一创新方法有望为更多癌症患者带来福音,特别是在应对B-ALL和实体瘤的治疗挑战时。2025-03-29
-
 湖南科伦制药申报比拉斯汀口服溶液上市,抗过敏药物市场竞争激烈 2025年3月25日,湖南科伦制药有限公司成功提交了比拉斯汀口服溶液的上市申请,该申请已获得受理。比拉斯汀(Bilastine)是一种非镇静性、长效的第二代抗组胺药,广泛用于过敏性鼻炎和荨麻疹的症状缓解。 比拉斯汀药理特性与优势 比拉斯汀属于H1组胺受体拮抗剂,是一种高选择性的第二代抗组胺药,具有起效快、持续时间长的特点。与其他抗组胺药相比,比拉斯汀的H1受体亲和力更强,比西替利嗪高三倍,比非索非那定高六倍。此外,使用比拉斯汀治疗不会与CYP酶系统产生显著相互作用,且耐受性良好,副作用较低,是治疗过敏性疾病的优选药物。 比拉斯汀的市场发展与全球上市进程 比拉斯汀的原研产品由西班牙FAES制药公司开发,最早于2010年8月在欧盟上市。该药品被批准用于治疗成人和12岁以上青少年的荨麻疹及变应性鼻炎。根据公开资料,2023年6月,意大利美纳里尼集团推出的比拉斯汀片(商品名:力敏能®)获得国家药品监督管理局(NMPA)批准上市,适用于12岁以上青少年及成人的荨麻疹治疗。 此外,2024年11月,江苏华阳制药推出的比拉斯汀片(商品名:新敏特®)也顺利通过4类仿制药注册,成为国内首个过评的产品。随着国内药企的积极布局,目前已有多家企业,包括山东新时代、石家庄四药、华益药业等,向NMPA提交了比拉斯汀口服溶液的上市申请,市场竞争愈加激烈。 荨麻疹治疗需求与比拉斯汀口服溶液的市场前景 中国的慢性荨麻疹发病率已达到2.6%-4.2%,高于全球平均水平。慢性荨麻疹患者通常病程较长,且复发率较高,给患者带来巨大的健康负担。除此之外,荨麻疹还常伴随失眠、焦虑等心理问题,增加了患者的生活负担。因此,则需一种既高效又能被患者接受的治疗方法。 目前,第一代抗组胺药在治疗荨麻疹时常常伴随镇静、认知功能下降等副作用,影响患者的日常生活。而第二代抗组胺药,如比拉斯汀,因其低镇静性和不易产生抗胆碱作用,已成为新的治疗一线药物。比拉斯汀口服溶液剂型,特别适合儿童患者,能够准确提供药物剂量,提高服药的便利性和患者的依从性。 中国抗过敏药物市场潜力巨大 根据数据显示,2023年和2024年上半年,全国医院端抗组胺药物的销售额分别为50.94亿元和25.69亿元;全国药店零售端销售额则为26.25亿元和12.55亿元,市场潜力巨大。随着比拉斯汀口服溶液的推出,预计将进一步满足儿童和成人患者的需求,成为抗过敏药物市场的重要一员。 总结 比拉斯汀口服溶液的上市申报受理标志着该药物在中国市场的进一步推进,预计将在未来的抗过敏药物市场中占据重要位置。随着相关产品逐步获批上市,国内荨麻疹和过敏性鼻炎患者将迎来更多高效、安全的治疗选择。同时,这也为患者带来了更具个性化的治疗方案,满足了中国市场日益增长的医疗需求。
湖南科伦制药申报比拉斯汀口服溶液上市,抗过敏药物市场竞争激烈 2025年3月25日,湖南科伦制药有限公司成功提交了比拉斯汀口服溶液的上市申请,该申请已获得受理。比拉斯汀(Bilastine)是一种非镇静性、长效的第二代抗组胺药,广泛用于过敏性鼻炎和荨麻疹的症状缓解。 比拉斯汀药理特性与优势 比拉斯汀属于H1组胺受体拮抗剂,是一种高选择性的第二代抗组胺药,具有起效快、持续时间长的特点。与其他抗组胺药相比,比拉斯汀的H1受体亲和力更强,比西替利嗪高三倍,比非索非那定高六倍。此外,使用比拉斯汀治疗不会与CYP酶系统产生显著相互作用,且耐受性良好,副作用较低,是治疗过敏性疾病的优选药物。 比拉斯汀的市场发展与全球上市进程 比拉斯汀的原研产品由西班牙FAES制药公司开发,最早于2010年8月在欧盟上市。该药品被批准用于治疗成人和12岁以上青少年的荨麻疹及变应性鼻炎。根据公开资料,2023年6月,意大利美纳里尼集团推出的比拉斯汀片(商品名:力敏能®)获得国家药品监督管理局(NMPA)批准上市,适用于12岁以上青少年及成人的荨麻疹治疗。 此外,2024年11月,江苏华阳制药推出的比拉斯汀片(商品名:新敏特®)也顺利通过4类仿制药注册,成为国内首个过评的产品。随着国内药企的积极布局,目前已有多家企业,包括山东新时代、石家庄四药、华益药业等,向NMPA提交了比拉斯汀口服溶液的上市申请,市场竞争愈加激烈。 荨麻疹治疗需求与比拉斯汀口服溶液的市场前景 中国的慢性荨麻疹发病率已达到2.6%-4.2%,高于全球平均水平。慢性荨麻疹患者通常病程较长,且复发率较高,给患者带来巨大的健康负担。除此之外,荨麻疹还常伴随失眠、焦虑等心理问题,增加了患者的生活负担。因此,则需一种既高效又能被患者接受的治疗方法。 目前,第一代抗组胺药在治疗荨麻疹时常常伴随镇静、认知功能下降等副作用,影响患者的日常生活。而第二代抗组胺药,如比拉斯汀,因其低镇静性和不易产生抗胆碱作用,已成为新的治疗一线药物。比拉斯汀口服溶液剂型,特别适合儿童患者,能够准确提供药物剂量,提高服药的便利性和患者的依从性。 中国抗过敏药物市场潜力巨大 根据数据显示,2023年和2024年上半年,全国医院端抗组胺药物的销售额分别为50.94亿元和25.69亿元;全国药店零售端销售额则为26.25亿元和12.55亿元,市场潜力巨大。随着比拉斯汀口服溶液的推出,预计将进一步满足儿童和成人患者的需求,成为抗过敏药物市场的重要一员。 总结 比拉斯汀口服溶液的上市申报受理标志着该药物在中国市场的进一步推进,预计将在未来的抗过敏药物市场中占据重要位置。随着相关产品逐步获批上市,国内荨麻疹和过敏性鼻炎患者将迎来更多高效、安全的治疗选择。同时,这也为患者带来了更具个性化的治疗方案,满足了中国市场日益增长的医疗需求。2025-03-29
-
 突破性进展!卡博替尼获批用于治疗神经内分泌肿瘤 3月26日,Exelixis宣布卡博替尼(CABOMETYX)获得 FDA批准 ,用于治疗那些曾接受过治疗的、不可切除的局部晚期或转移性的、分化良好的胰腺神经内分泌肿瘤(pNET)和 胰腺外神经内分泌肿瘤(epNET)的成人和儿童(≥12岁)患者。这是全球首个被批准用于治疗无论原发肿瘤部位、分级、生长抑素受体表达与功能状态的 经治神经内分泌肿瘤(NET)的药物。 III期研究结果支持批准 此次批准的依据是III期CABINET(A021602)研究的积极结果。该多中心、随机、双盲、安慰剂对照的临床试验(n=298,99例pNET,199例epNET)评估了卡博替尼(60mg)对比安慰剂治疗已经接受至少一次治疗的pNET(99例)和epNET(199例)患者的 有效性和安全性 。该研究的主要终点是盲法独立中心审查(BICR)的无进展生存期(PFS) 。 研究结果显示: 在epNET 组,卡博替尼患者的PFS 显著延长(8.4 vs 3.9个月,HR=0.38,P<0.001),确认的客观缓解率 (cORR)较高(5% vs 0%); 在pNET 组,卡博替尼患者的PFS 也显著延长(13.8 vs 4.4个月,HR=0.23,P<0.001),cORR 为19%,明显高于安慰剂组的0%。 卡博替尼的多个适应症 卡博替尼是Exelixis 公司开发的一款小分子靶向药物,能够靶向多个受体酪氨酸激酶。在2012年11月获得FDA批准上市,目前已在美国获得批准的适应症包括: 进展性转移性甲状腺髓样癌(MTC) ; 既往接受过抗血管生成治疗的晚期肾细胞癌(RCC) ; 晚期肾细胞癌(RCC) ; 联合纳武利尤单抗治疗晚期RCC ; 治疗既往接受过索拉非尼治疗的肝细胞癌(HCC) ; 治疗既往接受过VEGFR靶向治疗且放射性碘难治性或不适用放射性碘的局部晚期或转移性分化型甲状腺癌(DTC) ; 治疗既往接受过治疗、不可切除的局部晚期或转移性的分化良好的胰腺神经内分泌肿瘤(pNET)和胰腺外神经内分泌肿瘤(epNET) 。 神经内分泌肿瘤(NET)概况 神经内分泌肿瘤(NET)是由人体消化道神经内分泌细胞 和其他器官(如肺、胰腺等)衍生的异质性肿瘤。虽然这种肿瘤可能发生在身体任何部位,但最常见的是胃肠道或肺部。 晚期胃肠道NET 和肺NET 患者的5年生存率分别为68%和55%。然而,胰腺神经内分泌肿瘤(pNET)通常具有较高的侵袭性,晚期患者的5年生存率仅为23%。大多数NET的生长较为缓慢,通常需要数年时间发展为晚期,但最终所有的晚期或转移性NET都将成为难治性和进展性疾病。 根据预计,2024年 美国的NET患者总数将超过38万例 ,其中大约有16.1万至19.2万例 患者将患有不可切除的局部晚期或转移性NET。 Exelixis的全球合作与市场布局 2016年,Exelixis将卡博替尼 在美国和日本以外的地区的开发与商业化独家授权给益普生(Ipsen) 。2017年,Exelixis则将卡博替尼在日本市场 的开发与商业化独家授权给了武田药品 。然而,Exelixis仍保留了在美国市场 的独家开发和商业化权利。 总结:卡博替尼为NET患者带来新希望 随着卡博替尼 的FDA批准,它成为了治疗不可切除的分化良好胰腺神经内分泌肿瘤 及胰腺外神经内分泌肿瘤 的首选靶向药物。该药物的批准为经治NET患者 提供了有效的治疗方案,并为今后治疗神经内分泌肿瘤的其他药物的研发提供了宝贵的参考和启示。 随着卡博替尼的不断发展和适应症的拓展,未来它可能会成为治疗NET患者的重要药物,帮助更多患者延长生命并提高生活质量。
突破性进展!卡博替尼获批用于治疗神经内分泌肿瘤 3月26日,Exelixis宣布卡博替尼(CABOMETYX)获得 FDA批准 ,用于治疗那些曾接受过治疗的、不可切除的局部晚期或转移性的、分化良好的胰腺神经内分泌肿瘤(pNET)和 胰腺外神经内分泌肿瘤(epNET)的成人和儿童(≥12岁)患者。这是全球首个被批准用于治疗无论原发肿瘤部位、分级、生长抑素受体表达与功能状态的 经治神经内分泌肿瘤(NET)的药物。 III期研究结果支持批准 此次批准的依据是III期CABINET(A021602)研究的积极结果。该多中心、随机、双盲、安慰剂对照的临床试验(n=298,99例pNET,199例epNET)评估了卡博替尼(60mg)对比安慰剂治疗已经接受至少一次治疗的pNET(99例)和epNET(199例)患者的 有效性和安全性 。该研究的主要终点是盲法独立中心审查(BICR)的无进展生存期(PFS) 。 研究结果显示: 在epNET 组,卡博替尼患者的PFS 显著延长(8.4 vs 3.9个月,HR=0.38,P<0.001),确认的客观缓解率 (cORR)较高(5% vs 0%); 在pNET 组,卡博替尼患者的PFS 也显著延长(13.8 vs 4.4个月,HR=0.23,P<0.001),cORR 为19%,明显高于安慰剂组的0%。 卡博替尼的多个适应症 卡博替尼是Exelixis 公司开发的一款小分子靶向药物,能够靶向多个受体酪氨酸激酶。在2012年11月获得FDA批准上市,目前已在美国获得批准的适应症包括: 进展性转移性甲状腺髓样癌(MTC) ; 既往接受过抗血管生成治疗的晚期肾细胞癌(RCC) ; 晚期肾细胞癌(RCC) ; 联合纳武利尤单抗治疗晚期RCC ; 治疗既往接受过索拉非尼治疗的肝细胞癌(HCC) ; 治疗既往接受过VEGFR靶向治疗且放射性碘难治性或不适用放射性碘的局部晚期或转移性分化型甲状腺癌(DTC) ; 治疗既往接受过治疗、不可切除的局部晚期或转移性的分化良好的胰腺神经内分泌肿瘤(pNET)和胰腺外神经内分泌肿瘤(epNET) 。 神经内分泌肿瘤(NET)概况 神经内分泌肿瘤(NET)是由人体消化道神经内分泌细胞 和其他器官(如肺、胰腺等)衍生的异质性肿瘤。虽然这种肿瘤可能发生在身体任何部位,但最常见的是胃肠道或肺部。 晚期胃肠道NET 和肺NET 患者的5年生存率分别为68%和55%。然而,胰腺神经内分泌肿瘤(pNET)通常具有较高的侵袭性,晚期患者的5年生存率仅为23%。大多数NET的生长较为缓慢,通常需要数年时间发展为晚期,但最终所有的晚期或转移性NET都将成为难治性和进展性疾病。 根据预计,2024年 美国的NET患者总数将超过38万例 ,其中大约有16.1万至19.2万例 患者将患有不可切除的局部晚期或转移性NET。 Exelixis的全球合作与市场布局 2016年,Exelixis将卡博替尼 在美国和日本以外的地区的开发与商业化独家授权给益普生(Ipsen) 。2017年,Exelixis则将卡博替尼在日本市场 的开发与商业化独家授权给了武田药品 。然而,Exelixis仍保留了在美国市场 的独家开发和商业化权利。 总结:卡博替尼为NET患者带来新希望 随着卡博替尼 的FDA批准,它成为了治疗不可切除的分化良好胰腺神经内分泌肿瘤 及胰腺外神经内分泌肿瘤 的首选靶向药物。该药物的批准为经治NET患者 提供了有效的治疗方案,并为今后治疗神经内分泌肿瘤的其他药物的研发提供了宝贵的参考和启示。 随着卡博替尼的不断发展和适应症的拓展,未来它可能会成为治疗NET患者的重要药物,帮助更多患者延长生命并提高生活质量。2025-03-28
-
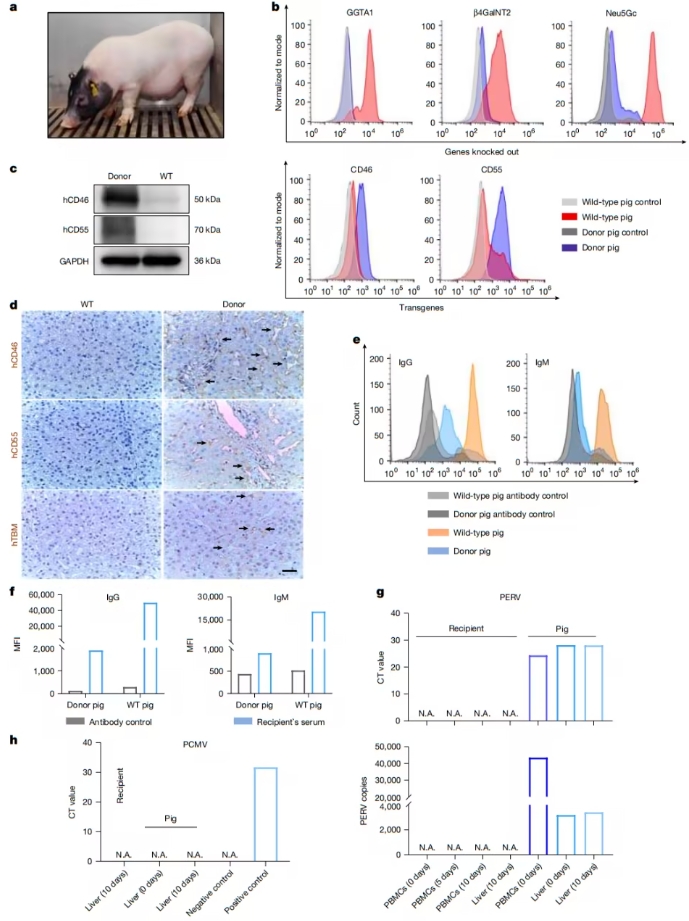 全球首例!基因编辑猪肝成功移植人体,运行十天无排异反应 近日,空军军医大学西京医院 窦科峰院士团队在国际权威期刊 Nature 发表研究论文,公布了世界首例基因编辑猪肝脏移植人体 的突破性进展。研究团队成功将经过基因改造的猪肝移植到一名脑死亡患者 体内,并监测其运行情况,结果表明,该器官在人体内存活并正常工作长达10天 ,且未出现明显的免疫排斥反应。这一研究为未来异种器官移植 提供了重要的理论基础,或将成为肝衰竭患者等待人类供体肝脏的过渡疗法 。 基因编辑猪肝移植:手术关键步骤 在严格的医院伦理监督 下,研究团队选择了一名生命体征稳定的脑死亡患者,采用异位辅助肝移植方案 ,即在不切除原有肝脏的情况下,将基因改造的巴马小型猪 肝脏移植入人体。手术过程包括以下关键步骤: 血管连接 :将猪肝的肝动脉 与患者腹主动脉 对接,确保血流供应; 静脉回流 :猪肝的门静脉 连接至患者下腔静脉 ; 胆汁引流 :建立外部胆汁排放通道 ,监测胆汁分泌情况。 移植后10天:猪肝运行稳定,功能正常 移植后,研究团队持续监测肝功能、血流动力学及免疫反应 ,结果显示: 胆汁分泌 :移植2小时后,猪肝开始产生金黄色胆汁 ,10天内累计分泌66.5毫升 ; 蛋白合成 :猪血清白蛋白水平持续升高,提示肝脏合成功能正常 ; 血流稳定 :肝动脉血流速度稳定在41.45-60.63 cm/s ; 无严重排斥 :组织检查显示,移植肝脏再生良好 ,未出现典型的免疫排斥反应 。 这些结果表明,基因编辑猪肝能够在人体内正常运作 ,为异种器官移植的进一步临床应用奠定了基础。 突破免疫排斥难题:六基因改造技术 异种器官移植的最大挑战在于免疫排斥反应 。直接移植猪器官会导致超急性排斥 ,因为猪细胞表面的α-半乳糖抗原 会引发人体免疫系统的强烈攻击。为此,中国科研团队采用六基因编辑技术 ,改造供体猪(巴马小型猪): 三大“排异因子”基因敲除 : GTKO :去除α-半乳糖抗原,减少超急性排斥; CMAH :抑制新抗原合成,降低免疫攻击; B4GALNT2 :减少免疫识别,提高生存率。 三重“保护盾”基因植入 : hCD46、hCD55 :调节补体系统,抑制免疫攻击; hTBM :防止凝血失衡,提高肝脏存活率。 这些基因改造使得猪肝能够更好地适应人体环境 ,显著降低了排异反应。 免疫“攻防战”:精准抑制排异 为了进一步控制免疫排斥,研究团队制定了多靶点免疫抑制方案 : 术前 :使用抗胸腺细胞球蛋白 清除T细胞,并应用补体抑制剂 防止超急性排斥; 术后 :联合他克莫司、霉酚酸酯 (经典抗排异药)+ 利妥昔单抗 (抑制B细胞活化)。 监测结果显示: T细胞活性被有效抑制 ; B细胞在术后第3天短暂激活 ,但及时受到控制 ; 炎症因子(IL-6、TNF-α)维持低水平 ,补体沉积极少。 这一免疫调控策略,使猪肝在人体内实现了稳定存活 。 未来展望:猪肝或成肝衰竭患者的“生命桥梁” 全球每年有数百万肝病患者 因等待不到供体而失去生命。我国每年新增30万-50万肝衰竭患者 ,但真正能接受人类肝脏移植的人数极为有限。基因编辑猪肝移植 的成功,意味着未来可能为这些患者提供替代或过渡治疗 方案。 研究团队计划: 延长移植存活时间 ,观察长期效果; 探索原位移植方案 (彻底替换病变肝脏); 优化基因编辑技术 ,进一步降低排异风险。 生物医学新时代:定制化猪器官或将成为现实 近年来,异种移植技术飞速发展 ,从猪心脏、猪肾脏 到猪肝脏 ,基因编辑技术不断完善,使“定制化器官”成为可能。提供本次实验供体猪的成都中科奥格生物科技有限公司 ,正致力于打造未来器官工厂 ,研发用于人体移植的猪器官、生物医用材料 等。 潘登科研究员表示,中科奥格采用的六基因编辑技术 与美国Revivicor公司开发的十基因编辑猪 有所不同,但均在临床研究中表现出良好效果。值得一提的是,巴马小型猪的器官大小与人类更接近 ,无需进行额外的生长基因敲除,使其更适合移植应用。 总结:医学历史性突破,未来可期 这项全球首例基因编辑猪肝移植研究 表明: 基因改造猪肝能够在人体内正常存活 ,无明显排异; 凝血机制趋于正常 ,避免了异种移植中的常见风险; 提供急性肝衰竭的过渡治疗新方案 ,可能拯救大量等待供体的患者。 随着基因编辑、免疫调控和外科移植技术的进步 ,异种器官移植将加速向临床应用迈进。未来,定制化猪器官移植或将彻底改写医学历史 ,为无数患者带来新生希望。
全球首例!基因编辑猪肝成功移植人体,运行十天无排异反应 近日,空军军医大学西京医院 窦科峰院士团队在国际权威期刊 Nature 发表研究论文,公布了世界首例基因编辑猪肝脏移植人体 的突破性进展。研究团队成功将经过基因改造的猪肝移植到一名脑死亡患者 体内,并监测其运行情况,结果表明,该器官在人体内存活并正常工作长达10天 ,且未出现明显的免疫排斥反应。这一研究为未来异种器官移植 提供了重要的理论基础,或将成为肝衰竭患者等待人类供体肝脏的过渡疗法 。 基因编辑猪肝移植:手术关键步骤 在严格的医院伦理监督 下,研究团队选择了一名生命体征稳定的脑死亡患者,采用异位辅助肝移植方案 ,即在不切除原有肝脏的情况下,将基因改造的巴马小型猪 肝脏移植入人体。手术过程包括以下关键步骤: 血管连接 :将猪肝的肝动脉 与患者腹主动脉 对接,确保血流供应; 静脉回流 :猪肝的门静脉 连接至患者下腔静脉 ; 胆汁引流 :建立外部胆汁排放通道 ,监测胆汁分泌情况。 移植后10天:猪肝运行稳定,功能正常 移植后,研究团队持续监测肝功能、血流动力学及免疫反应 ,结果显示: 胆汁分泌 :移植2小时后,猪肝开始产生金黄色胆汁 ,10天内累计分泌66.5毫升 ; 蛋白合成 :猪血清白蛋白水平持续升高,提示肝脏合成功能正常 ; 血流稳定 :肝动脉血流速度稳定在41.45-60.63 cm/s ; 无严重排斥 :组织检查显示,移植肝脏再生良好 ,未出现典型的免疫排斥反应 。 这些结果表明,基因编辑猪肝能够在人体内正常运作 ,为异种器官移植的进一步临床应用奠定了基础。 突破免疫排斥难题:六基因改造技术 异种器官移植的最大挑战在于免疫排斥反应 。直接移植猪器官会导致超急性排斥 ,因为猪细胞表面的α-半乳糖抗原 会引发人体免疫系统的强烈攻击。为此,中国科研团队采用六基因编辑技术 ,改造供体猪(巴马小型猪): 三大“排异因子”基因敲除 : GTKO :去除α-半乳糖抗原,减少超急性排斥; CMAH :抑制新抗原合成,降低免疫攻击; B4GALNT2 :减少免疫识别,提高生存率。 三重“保护盾”基因植入 : hCD46、hCD55 :调节补体系统,抑制免疫攻击; hTBM :防止凝血失衡,提高肝脏存活率。 这些基因改造使得猪肝能够更好地适应人体环境 ,显著降低了排异反应。 免疫“攻防战”:精准抑制排异 为了进一步控制免疫排斥,研究团队制定了多靶点免疫抑制方案 : 术前 :使用抗胸腺细胞球蛋白 清除T细胞,并应用补体抑制剂 防止超急性排斥; 术后 :联合他克莫司、霉酚酸酯 (经典抗排异药)+ 利妥昔单抗 (抑制B细胞活化)。 监测结果显示: T细胞活性被有效抑制 ; B细胞在术后第3天短暂激活 ,但及时受到控制 ; 炎症因子(IL-6、TNF-α)维持低水平 ,补体沉积极少。 这一免疫调控策略,使猪肝在人体内实现了稳定存活 。 未来展望:猪肝或成肝衰竭患者的“生命桥梁” 全球每年有数百万肝病患者 因等待不到供体而失去生命。我国每年新增30万-50万肝衰竭患者 ,但真正能接受人类肝脏移植的人数极为有限。基因编辑猪肝移植 的成功,意味着未来可能为这些患者提供替代或过渡治疗 方案。 研究团队计划: 延长移植存活时间 ,观察长期效果; 探索原位移植方案 (彻底替换病变肝脏); 优化基因编辑技术 ,进一步降低排异风险。 生物医学新时代:定制化猪器官或将成为现实 近年来,异种移植技术飞速发展 ,从猪心脏、猪肾脏 到猪肝脏 ,基因编辑技术不断完善,使“定制化器官”成为可能。提供本次实验供体猪的成都中科奥格生物科技有限公司 ,正致力于打造未来器官工厂 ,研发用于人体移植的猪器官、生物医用材料 等。 潘登科研究员表示,中科奥格采用的六基因编辑技术 与美国Revivicor公司开发的十基因编辑猪 有所不同,但均在临床研究中表现出良好效果。值得一提的是,巴马小型猪的器官大小与人类更接近 ,无需进行额外的生长基因敲除,使其更适合移植应用。 总结:医学历史性突破,未来可期 这项全球首例基因编辑猪肝移植研究 表明: 基因改造猪肝能够在人体内正常存活 ,无明显排异; 凝血机制趋于正常 ,避免了异种移植中的常见风险; 提供急性肝衰竭的过渡治疗新方案 ,可能拯救大量等待供体的患者。 随着基因编辑、免疫调控和外科移植技术的进步 ,异种器官移植将加速向临床应用迈进。未来,定制化猪器官移植或将彻底改写医学历史 ,为无数患者带来新生希望。2025-03-28
-
 新突破!谷美替尼联合疗法获批用于晚期非小细胞肺癌 3月25日,海和药物宣布其自主研发的新药谷美替尼片获得中国国家药品监督管理局(CDE)的临床批准。此新适应症用于联合甲磺酸奥希替尼片治疗未经系统治疗的EGFR敏感突变伴MET扩增或过表达的晚期非小细胞肺癌(NSCLC)。该联合治疗方案在临床研究中表现出了显著的疗效和可控的安全性,为患者提供了新的治疗选择。 谷美替尼:一种新型MET抑制剂 谷美替尼(SCC244)是海和药物开发的一款口服小分子MET抑制剂,具有高选择性和强效的特点。目前,谷美替尼已在国内获批用于治疗具有MET外显子14跳变的局部晚期或转移性非小细胞肺癌。谷美替尼的临床研究还在美国和日本展开,进一步验证其疗效和安全性,具有广泛的国际市场潜力。 海和药物的创新药物研发管线 上海海和药物研究开发股份有限公司,专注于创新药物的研发,特别是在抗肿瘤药物领域取得了多项突破。海和药物的产品管线丰富,涵盖了多种针对不同癌症类型的创新药物。公司目前在研的主要药物包括: HH2853 :这是一款高选择性、强效的EZH1/2双重抑制剂,与中科院上海药物研究所联合开发,目前处于2期临床试验阶段。与该靶点相关的在研药物还包括恒瑞医药的SHR2554和信诺维医药的XNW-5004。 CYH33 :这款药物是海和药物与中科院上海药物研究所合作研发的PI3Kα选择性抑制剂,属于一种全新结构的高活性小分子药物。临床研究结果表明,CYH33对乳腺癌、子宫内膜癌等具有PI3Kα突变的晚期实体瘤有效,且安全性良好,目前正处于2期临床试验阶段。 海和药物:创新驱动的未来 海和药物凭借其强大的自主研发能力和国际视野,致力于推动肿瘤治疗领域的创新。除了谷美替尼片外,海和药物的在研管线还包括CYH33和HH2853等创新药物。未来,随着这些在研药物逐步进入关键临床阶段,海和药物有望为全球患者带来新的治疗选择,进一步提升患者的生存率和生活质量。 展望未来 海和药物的创新药物和丰富的研发管线展示了其在抗肿瘤治疗领域的强大实力。随着多个在研药物进入临床关键阶段,海和药物预计将为患者提供更多治疗方案,推动全球癌症治疗的进步。
新突破!谷美替尼联合疗法获批用于晚期非小细胞肺癌 3月25日,海和药物宣布其自主研发的新药谷美替尼片获得中国国家药品监督管理局(CDE)的临床批准。此新适应症用于联合甲磺酸奥希替尼片治疗未经系统治疗的EGFR敏感突变伴MET扩增或过表达的晚期非小细胞肺癌(NSCLC)。该联合治疗方案在临床研究中表现出了显著的疗效和可控的安全性,为患者提供了新的治疗选择。 谷美替尼:一种新型MET抑制剂 谷美替尼(SCC244)是海和药物开发的一款口服小分子MET抑制剂,具有高选择性和强效的特点。目前,谷美替尼已在国内获批用于治疗具有MET外显子14跳变的局部晚期或转移性非小细胞肺癌。谷美替尼的临床研究还在美国和日本展开,进一步验证其疗效和安全性,具有广泛的国际市场潜力。 海和药物的创新药物研发管线 上海海和药物研究开发股份有限公司,专注于创新药物的研发,特别是在抗肿瘤药物领域取得了多项突破。海和药物的产品管线丰富,涵盖了多种针对不同癌症类型的创新药物。公司目前在研的主要药物包括: HH2853 :这是一款高选择性、强效的EZH1/2双重抑制剂,与中科院上海药物研究所联合开发,目前处于2期临床试验阶段。与该靶点相关的在研药物还包括恒瑞医药的SHR2554和信诺维医药的XNW-5004。 CYH33 :这款药物是海和药物与中科院上海药物研究所合作研发的PI3Kα选择性抑制剂,属于一种全新结构的高活性小分子药物。临床研究结果表明,CYH33对乳腺癌、子宫内膜癌等具有PI3Kα突变的晚期实体瘤有效,且安全性良好,目前正处于2期临床试验阶段。 海和药物:创新驱动的未来 海和药物凭借其强大的自主研发能力和国际视野,致力于推动肿瘤治疗领域的创新。除了谷美替尼片外,海和药物的在研管线还包括CYH33和HH2853等创新药物。未来,随着这些在研药物逐步进入关键临床阶段,海和药物有望为全球患者带来新的治疗选择,进一步提升患者的生存率和生活质量。 展望未来 海和药物的创新药物和丰富的研发管线展示了其在抗肿瘤治疗领域的强大实力。随着多个在研药物进入临床关键阶段,海和药物预计将为患者提供更多治疗方案,推动全球癌症治疗的进步。2025-03-28
-
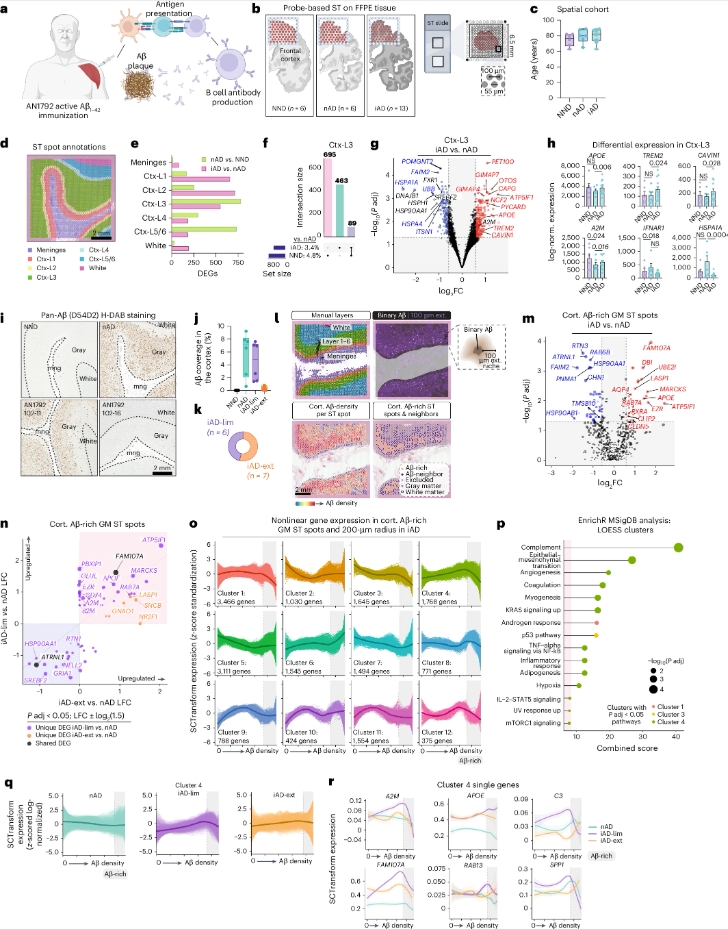 研究揭示大脑免疫细胞的新作用:对抗阿尔茨海默病的潜力 阿尔茨海默病(AD)长期以来一直是医学界的难题,随着患者年龄的增长,病情逐渐加重,尤其是记忆和认知功能的丧失。尽管多年来科学家们致力于清除大脑中的淀粉样β蛋白(Aβ)斑块来治疗这种疾病,但这一方法的疗效一直有限,且常常伴随副作用。近期,一项刊登在《Nature Medicine》杂志的研究为我们提供了一种新的治疗方向,利用大脑的免疫细胞来增强斑块清除能力,从而改善阿尔茨海默病。 小胶质细胞:大脑的免疫卫士 这项研究的最大亮点在于揭示了小胶质细胞在阿尔茨海默病治疗中的新作用。小胶质细胞作为大脑中的免疫细胞,通常负责清除外来病原和废物。在阿尔茨海默病中,它们不仅能清除淀粉样斑块,还能在清除斑块后帮助恢复大脑的正常功能,甚至有助于大脑自我修复。研究显示,强化小胶质细胞的功能可能成为一种新的治疗策略,有望改善甚至逆转阿尔茨海默病的进程。 空间转录组学技术揭示免疫细胞的行为差异 为了更好地理解这些免疫细胞的功能,研究团队采用了空间转录组学这一尖端技术,对接受过免疫治疗的阿尔茨海默病患者大脑组织样本进行了精确分析。这种技术可以在空间上定位基因的活跃区域,帮助研究人员观察小胶质细胞在不同大脑区域和免疫治疗下的反应。结果显示,虽然大多数小胶质细胞能有效清除斑块,但它们在不同患者的大脑中表现不一。有些小胶质细胞清除斑块的效率很高,而另一些则未能发挥应有的作用。 个体化治疗:根据基因特征定制治疗方案 研究还发现,某些基因(如TREM2和APOE)对免疫治疗的反应更为敏感,能够帮助小胶质细胞更好地清除淀粉样β蛋白斑块。这一发现为未来的个体化治疗提供了新的思路。科学家认为,若能识别出哪些患者的免疫细胞更容易响应治疗,或许可以绕过传统药物治疗,直接靶向这些免疫细胞,从而提高治疗的效果并减少副作用。 斑块清除和tau蛋白病理变化的关系 阿尔茨海默病的病理特征之一是淀粉样斑块和tau蛋白的积累。研究者指出,清除淀粉样β蛋白斑块能够在tau蛋白病理变化出现之前阻止病理进程的发生,从而避免进一步的认知损害。对于已经出现tau蛋白病理变化的患者,尽管淀粉样β蛋白仍然可以清除,但治疗的效果会大打折扣。因此,研究者建议,在阿尔茨海默病的早期阶段进行免疫治疗,可能会更有效地防止病情恶化。 免疫治疗的双刃剑:平衡免疫反应至关重要 尽管研究显示,小胶质细胞在治疗中的作用至关重要,但研究者也提醒,免疫反应的激活需要精准控制。过度的免疫激活可能会导致大脑肿胀等副作用,而过于温和的反应则可能无法达到治疗效果。因此,未来的治疗可能需要根据患者的具体情况来定制方案。有些患者可能需要更强的免疫刺激,而另一些则可能需要更温和的治疗以避免免疫过度反应。 前景展望:新靶点和新策略 这项研究不仅揭示了小胶质细胞在阿尔茨海默病治疗中的重要角色,也为未来的治疗提供了新的靶点。通过增强这些免疫细胞的功能,我们或许能够更有效地清除大脑中的淀粉样β蛋白斑块,从而延缓甚至阻止阿尔茨海默病的进展。此外,随着技术的进步,科学家们逐步揭示出不同大脑区域和免疫治疗方案下的免疫细胞反应差异,这也为个体化治疗提供了新的方向。 结语 阿尔茨海默病的治疗一直是医学界的难题,尽管现有的药物治疗效果有限,但通过这项最新的研究,我们看到了希望。通过精准激活大脑免疫细胞、清除斑块并恢复大脑健康,未来可能会带来革命性的治疗突破。更重要的是,个体化治疗策略的实施可能会极大提升治疗效果,为广大的阿尔茨海默病患者带来新的福音。
研究揭示大脑免疫细胞的新作用:对抗阿尔茨海默病的潜力 阿尔茨海默病(AD)长期以来一直是医学界的难题,随着患者年龄的增长,病情逐渐加重,尤其是记忆和认知功能的丧失。尽管多年来科学家们致力于清除大脑中的淀粉样β蛋白(Aβ)斑块来治疗这种疾病,但这一方法的疗效一直有限,且常常伴随副作用。近期,一项刊登在《Nature Medicine》杂志的研究为我们提供了一种新的治疗方向,利用大脑的免疫细胞来增强斑块清除能力,从而改善阿尔茨海默病。 小胶质细胞:大脑的免疫卫士 这项研究的最大亮点在于揭示了小胶质细胞在阿尔茨海默病治疗中的新作用。小胶质细胞作为大脑中的免疫细胞,通常负责清除外来病原和废物。在阿尔茨海默病中,它们不仅能清除淀粉样斑块,还能在清除斑块后帮助恢复大脑的正常功能,甚至有助于大脑自我修复。研究显示,强化小胶质细胞的功能可能成为一种新的治疗策略,有望改善甚至逆转阿尔茨海默病的进程。 空间转录组学技术揭示免疫细胞的行为差异 为了更好地理解这些免疫细胞的功能,研究团队采用了空间转录组学这一尖端技术,对接受过免疫治疗的阿尔茨海默病患者大脑组织样本进行了精确分析。这种技术可以在空间上定位基因的活跃区域,帮助研究人员观察小胶质细胞在不同大脑区域和免疫治疗下的反应。结果显示,虽然大多数小胶质细胞能有效清除斑块,但它们在不同患者的大脑中表现不一。有些小胶质细胞清除斑块的效率很高,而另一些则未能发挥应有的作用。 个体化治疗:根据基因特征定制治疗方案 研究还发现,某些基因(如TREM2和APOE)对免疫治疗的反应更为敏感,能够帮助小胶质细胞更好地清除淀粉样β蛋白斑块。这一发现为未来的个体化治疗提供了新的思路。科学家认为,若能识别出哪些患者的免疫细胞更容易响应治疗,或许可以绕过传统药物治疗,直接靶向这些免疫细胞,从而提高治疗的效果并减少副作用。 斑块清除和tau蛋白病理变化的关系 阿尔茨海默病的病理特征之一是淀粉样斑块和tau蛋白的积累。研究者指出,清除淀粉样β蛋白斑块能够在tau蛋白病理变化出现之前阻止病理进程的发生,从而避免进一步的认知损害。对于已经出现tau蛋白病理变化的患者,尽管淀粉样β蛋白仍然可以清除,但治疗的效果会大打折扣。因此,研究者建议,在阿尔茨海默病的早期阶段进行免疫治疗,可能会更有效地防止病情恶化。 免疫治疗的双刃剑:平衡免疫反应至关重要 尽管研究显示,小胶质细胞在治疗中的作用至关重要,但研究者也提醒,免疫反应的激活需要精准控制。过度的免疫激活可能会导致大脑肿胀等副作用,而过于温和的反应则可能无法达到治疗效果。因此,未来的治疗可能需要根据患者的具体情况来定制方案。有些患者可能需要更强的免疫刺激,而另一些则可能需要更温和的治疗以避免免疫过度反应。 前景展望:新靶点和新策略 这项研究不仅揭示了小胶质细胞在阿尔茨海默病治疗中的重要角色,也为未来的治疗提供了新的靶点。通过增强这些免疫细胞的功能,我们或许能够更有效地清除大脑中的淀粉样β蛋白斑块,从而延缓甚至阻止阿尔茨海默病的进展。此外,随着技术的进步,科学家们逐步揭示出不同大脑区域和免疫治疗方案下的免疫细胞反应差异,这也为个体化治疗提供了新的方向。 结语 阿尔茨海默病的治疗一直是医学界的难题,尽管现有的药物治疗效果有限,但通过这项最新的研究,我们看到了希望。通过精准激活大脑免疫细胞、清除斑块并恢复大脑健康,未来可能会带来革命性的治疗突破。更重要的是,个体化治疗策略的实施可能会极大提升治疗效果,为广大的阿尔茨海默病患者带来新的福音。2025-03-26
大家都在看
药品推荐
-
艾伏尼布 Ivosidenib
白血病1年持续缓解62%,提高胆管癌无进展生存期
中国基石药业
-
古塞奇尤单抗 guselkumab
适用为成年患者有中度-至-严重斑块性银屑病的治疗患者是全身治疗或光治疗后备者
美国杨森
-

阿奇霉素 Azithromycin
本品适用于敏感细菌所引起的下列感染:1.支气管炎、肺炎等下呼吸道感染;2.皮肤和软组织感染;急性中耳炎;3.鼻窦炎、咽炎、扁桃体炎等上呼吸道感染等
印度Aprazer Healthcare Private Limited
-

加巴喷丁 Gabapentin
用于治疗中至重度多动腿综合症(RLS)
英国葛兰素史克(GSK Plc)
-
奥拉帕利 Olaparib
新型的PARP抑制剂,用于治疗晚期卵巢癌,乳腺癌等
孟加拉碧康制药股份有限公司


