乳腺癌微环境中的精氨酸代谢与免疫逃逸机制研究
 搜医药
搜医药
关键词: #健康资讯
 搜医药
搜医药
关键词: #健康资讯
中国科学院杭州医学研究所的胡海教授及其研究团队,近日阐明了乳腺癌微环境中肿瘤细胞与免疫细胞之间如何通过精氨酸代谢进行协作,促进免疫逃逸的分子机制,为联合免疫治疗提供了新的靶点。
肿瘤微环境中的代谢交互与免疫逃逸
肿瘤微环境(TME)是一个复杂的细胞生态系统,其中不同类型的细胞之间通过代谢交互网络相互影响,进而调控肿瘤的发生与发展。此次研究采用单细胞测序和代谢组学分析技术,揭示了乳腺癌细胞通过分泌精氨酸,诱导肿瘤相关巨噬细胞(TAM)发生代谢重编程的机制。研究表明,乳腺癌细胞分泌的精氨酸会激活TAM内多胺合成通路,特别是精胺的过度合成,这一过程通过表观遗传机制调控,促使TAM转化为具有免疫抑制功能的表型。
精氨酸与肿瘤进展的关系
研究进一步发现,乳腺癌患者血清中的精氨酸水平与肿瘤进展密切相关。尤其是在免疫完整的情况下,精氨酸的促癌效应表现明显。值得注意的是,在免疫缺陷小鼠模型中,外源补充精氨酸并未促进肿瘤生长,这表明精氨酸的促癌作用主要通过调节免疫系统来实现。
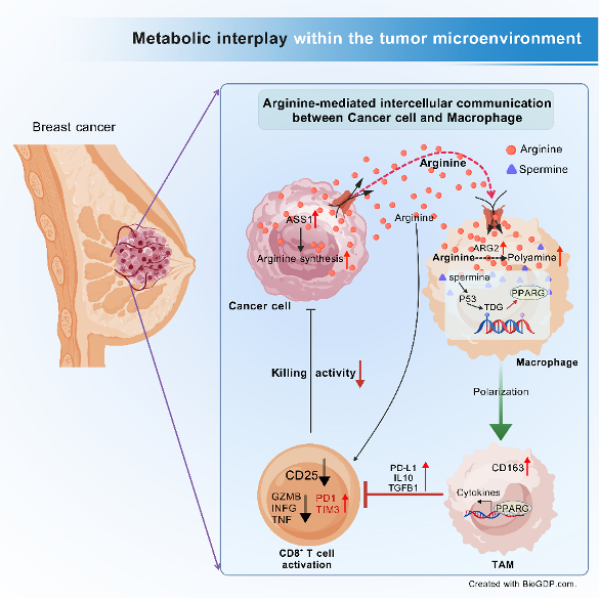
巨噬细胞内精胺的表观遗传调控
研究还揭示,TAM内精胺的积累通过调节DNA去甲基化酶的活性,重新塑造了关键免疫基因的表观遗传状态。这一过程使TAM分泌免疫抑制因子,抑制CD8+ T细胞的活化及功能,从而促进免疫逃逸。
靶向代谢轴的临床潜力
通过使用FDA批准的多胺合成抑制剂DFMO,研究团队成功地阻断了精氨酸-多胺代谢轴,逆转了肿瘤微环境的免疫抑制状态,并有效抑制了肿瘤的进展。该研究为靶向代谢途径以增强现有免疫治疗提供了新思路,并为相关的临床试验奠定了基础。
研究成果的发表与前景
该项研究成果于4月3日在线发表在《癌细胞》(Cancer Cell)杂志上,题为“Cancer cell-derived arginine fuels polyamine biosynthesis in tumor-associated macrophages to promote immune evasion”。目前,基于这一发现,相关的临床试验正在积极筹备中,未来可能为乳腺癌患者提供更有效的治疗方案。
结论:代谢调控促进免疫逃逸
本研究不仅揭示了精氨酸代谢在肿瘤免疫逃逸中的关键作用,也为精准治疗提供了新的视角。通过干预肿瘤细胞与TAM之间的代谢轴,能够显著增强免疫治疗的效果,为癌症治疗的临床应用带来新的希望。

2025-04-13

2025-04-13

2025-04-13
2025-04-13
2025-04-13