癌症治疗新突破:翻译组疗法精准靶向癌基因,前列腺癌治疗迎来新曙光
 搜医药
搜医药
关键词: #健康资讯
 搜医药
搜医药
关键词: #健康资讯
前列腺癌(PCa)是男性常见的癌症之一,且是导致男性癌症死亡的主要原因。虽然雄激素信号疗法在初期能够带来一定的治疗效果,但多数患者最终都会发展为去势抵抗前列腺癌(CRPC),此时肿瘤具有更高的转移性和死亡率,令患者面临极大的治疗挑战。近年来,来自加州大学旧金山分校的科研团队发现了一种新型药物——zotatifin,可能成为突破这一难题的关键武器。
小分子药物Zotatifin:锁定癌细胞翻译机制
2025年3月20日,科研团队在《Cancer Cell》期刊发表了题为“Small-molecule RNA therapeutics to target prostate cancer”的研究成果。研究显示,zotatifin通过靶向真核起始因子eIF4A,抑制特定致癌基因mRNA(如AR、AR-v7和HIF1α)的翻译,提出了一种全新的治疗理念——“翻译组疗法”(translatome therapy)。这种新疗法通过干扰癌细胞的“翻译工厂”,阻止癌基因的蛋白质合成,从而为治疗前列腺癌开辟了新的方向。

eIF4A:癌细胞翻译工厂的核心
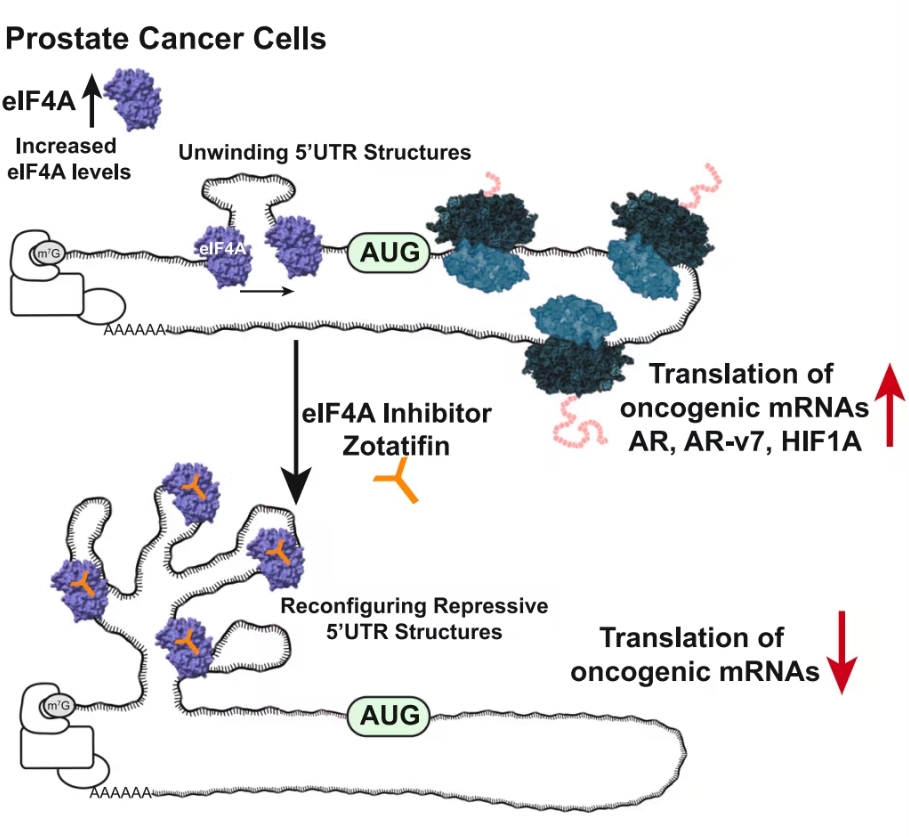
在癌细胞内,真核起始因子eIF4A发挥着至关重要的作用,它是RNA解旋酶,负责解开mRNA的5'非翻译区(5'UTR),为核糖体的蛋白质合成提供支持。研究人员通过对370名患者样本的分析发现,eIF4A在转移性前列腺癌中异常活跃。高表达的患者15年生存率大幅下降,进一步表明eIF4A可能是前列腺癌治疗的关键靶点。
Zotatifin:精准干扰癌细胞蛋白合成
zotatifin作为一款小分子药物,被比作“分子胶水”,它能够精确地粘住eIF4A的活性位点,阻止其解开致癌基因的RNA结构。研究团队发现,zotatifin在多个方面表现出显著疗效:
抑制雄激素受体(AR) :在去势抵抗性前列腺癌(CRPC)模型中,zotatifin能够有效抑制雄激素受体及其耐药变体AR-v7的蛋白合成,切断癌细胞的“激素引擎”。
破坏癌细胞的缺氧适应性 :在模拟肿瘤微环境的缺氧条件下,zotatifin使HIF1α蛋白的水平下降75%,有效破坏癌细胞的“应急供能系统”。
提高放疗效果 :当zotatifin与放疗联合使用时,肿瘤的消退速度增加了3倍。
翻译组疗法:重塑RNA结构的创新技术
研究团队使用先进的DMS-MaPSeq技术,捕捉到令人惊讶的分子重塑过程。zotatifin能改变特定致癌基因mRNA的结构,例如,雄激素受体(AR)基因的5'UTR原本错综复杂,但经zotatifin处理后,RNA结构变得简单整齐,使核糖体无法识别这些基因的翻译起始信号。这一结构上的改变堪比“分子整形术”,有效阻止了致癌基因的表达,同时对正常基因的RNA结构影响极小,展示了zotatifin的高度选择性。
临床前景:zotatifin进入临床二期试验
目前,zotatifin已经进入临床二期试验,早期数据表明患者对该药物的耐受性良好,未来有望为晚期前列腺癌患者带来新的治疗选择。这项研究的亮点包括:
Zotatifin作为eIF4A抑制剂,可以显著降低前列腺癌的肿瘤负荷;
它能够精准抑制特定致癌基因(如AR、AR-v7、HIF1α)的翻译;
Zotatifin在前列腺癌翻译组中重塑5'UTR的RNA结构,为癌症治疗开辟了新的方向;
“翻译组疗法”有望成为治疗致死性前列腺癌的重要突破。
未来展望:新疗法的广阔前景
研究团队未来计划在以下几个方向进行进一步突破:
动态RNA结构图谱 :利用人工智能开发预测模型,识别更多可靶向的致癌基因RNA,为精准治疗提供支持。
联合疗法的探索 :研究与PARP抑制剂、免疫检查点抑制剂等药物的协同效应,提升治疗效果。
液体活检 :通过检测血液中的AR、HIF1α翻译产物,实现个性化精准用药。
总结
这项研究不仅提出了“翻译组疗法”的新概念,更为前列腺癌等致死性肿瘤提供了全新的治疗策略。随着zotatifin等新型药物的研发,癌症治疗的未来将更加精准和个性化。

2025-04-03

2025-04-03

2025-04-03

2025-04-03
2025-04-03